Revista
• 24/06/2025MACRO-MICROCROPOROSIDADE E SULFATAÇÃO NAS ETAPAS DE FORMAÇÃO DAS PLACAS POSITIVAS E NEGATIVAS DA BATERIA CHUMBO-ÁCIDO
O Legado de Carlos Ventura D'Alkaine na Área de Baterias Chumbo-Ácido Este é o primeiro conteúdo de uma série dedicada aos estudos do Prof. Carlos Ventura D’Alkaine sobre baterias chumbo-ácido. A série reúne trechos e reflexões extraídas de suas apresentações em congressos e simpósios, muitos dos quais permaneceram restritos à comunidade técnica envolvida com a produção dessas baterias.
Em várias apresentações públicas, o Prof. D’Alkaine embasado nos trabalhos de seu grupo e nos artigos publicados pelo grupo do Prof. Pavlov1-4 apresentava os aspectos que ocorrem na etapa de formação das placas das baterias chumbo-ácido quando não está presente o processo de imersão prévia das placas na solução de ácido sulfúrico (processo conhecido por soaking).
A visão do Prof. D’Alkaine muito se insere dentro da forma como grupo do Prof. Pavlov descreve as etapas de formação, exceto que ele ressalta a presença de reações de estado sólido dentro da zona de reação e por isso introduz a importância do conhecimento da macro e microporosidade das placas formadas como parâmetros de controle das qualidades finais das placas.
Hoje é bem aceito que a etapa de formação de ambas as placas (estágio onde as placas estão polarizadas) ocorre em dois estágios, onde no primeiro há o processo de formação de sulfato de chumbo, conhecido por “sulfatação” (não confundir com o processo de “sulfatação” superficial que ocorre na etapa do “soaking”) e no segundo as transformações químicas e eletroquímicas em massas ativas das placas positivas (PAM) e negativas (NAM). Esses processos envolvem as chamadas reações zonais, ou seja, o avanço das reações por regiões preferenciais de acordo com a resistência dos materiais que vão sendo formados.
Ressaltamos que o conhecimento e controle dos estágios de formação são importantes para a qualidade da produção de baterias chumbo-ácido, especialmente naqueles processos produtivos que optam pela formação das baterias nas próprias caixas do produto e sem o processo conhecido por “tombamento” do eletrólito. Afirmamos isso porque são essas etapas que produzirão as características finais das placas formadas quanto às novas porosidades diferentes daquelas deixadas após o processo de cura.
Como os caminhos de reações sofrem influência das camadas iniciais o controle metrológico passa também pela etapa inicial conhecida por “soaking” (não discutida nesse artigo). Enfatizamos esse fato porque observamos que em muitos processos produtivos essa etapa não se encontra inclusa na planilha do controle de qualidade das fábricas que produzem esse tipo de bateria.
PLACAS POSITIVAS
Primeiro estágio: o primeiro estágio de formação é caracterizado por reações químicas e eletroquímicas provocadas pela penetração da solução de ácido sulfúrico (H2SO4 + H2O) para o interior da placa. Assim, o material precursor, já empastado na grade e curado, é sulfatado com a diminuição da concentração de ácido formador da solução. Este primeiro estágio é assim denominado porque dá origem ao PbSO4 por meio de uma reação química da solução ácida com o precursor. O consumo de ácido sulfúrico provoca o aparecimento de um gradiente de concentração fazendo com que este se difunda do seio da solução para o interior da placa através dos macroporos presentes no material precursor formado na etapa da cura das placas. Nessas reações zonais já se pode ver que a macroporosidade anterior do material precursor se modifica com a formação das camadas de sulfatos de chumbo. Ainda no primeiro estágio há a formação do ?-PbO2 que é formado pela oxidação do material precursor que possui pH alcalino em seus poros. Quando na presença da etapa de soaking, esse primeiro estágio é afetado porque estamos agora frente não apenas às superfícies dos materiais precursores em si mas, também, a camadas de sulfatos de chumbo formadas previamente. Por isso que recomendamos que a etapa de “soaking” deva ter seus parâmetros conhecidos e controlados frente aos diferentes lotes de produção.
Segundo estágio. No segundo estágio há a reação eletroquímica de formação do ?-PbO2. Este processo consome água e produz ions H+, acidificando o meio. O ácido assim formado sai do material sólido da placa já transformado em ?-PbO2, aumentando a concentração de ácido da solução de formação. Durante este segundo estágio, o PbSO4 formado no primeiro estágio nas superfícies internas dos macroporos do material precursor (processo de sulfatação) é também oxidado para ?-PbO2, devido o aumento do meio ácido nessas regiões de superfície. Nessa etapa, um mecanismo de estado sólido é proposto para a formação final do PAM. A difusão e migração de íons são consideradas as etapas limitantes da taxa dos processos apresentando a razão ?/? PbO2 e a direção do crescimento zonal como parâmetros importantes que influenciarão a capacidade e o desempenho do ciclo de vida da bateria.
Assim, o controle das variáveis como temperatura, concentração do ácido, composição de fase da pasta curada, corrente de formação e tempo (aqui devemos incluir o tempo de “soaking”) presentes no primeiro estágio, caracterizado pelo avanço zonal da formação do PbSO4 e do ?-PbO2 são parâmetros importantes de controle de produção.
Nossos estudos e os artigos publicados principalmente pelo grupo do Prof.Pavlov nos permite afirmar que a capacidade da placa positiva é determinada pela estrutura do PAM e pela razão ?/? PbO2 . Devido à importância dessa etapa no processo de formação da placa positiva, tendo em conta o papel limitante que em geral essa placa exerce na operação das baterias chumbo-/ácido, é que os artigos do Prof.D’Alkaine exploram esse tema advindo dos resultados de vários trabalhos de mestrado e tese de doutorado, mostrando que a difusão do ácido durante o processo de formação contribui para a acidificação da solução de formação.
Estas são as razões pelas quais durante a formação são observados dois estágios. O primeiro em que predomina o consumo de ácido sulfúrico e um segundo em que a solução se torna mais ácida, chegando a ser ainda mais ácida do que no início do processo.
Com isso há as formações de ?- PbO2 e ?-PbO2, conforme o caso, que estão relacionadas à disponibilidade ácida do meio de reação. Isso foi por nós comprovado experimentalmente com os estudos da formação de filme anódico de PbO2 em eletrodos planos de Pb em diferentes concentrações de ácido sulfúrico.
Para concentrações molares maiores que 5,0 molL-1 de ácido sulfúrico foi encontrado como produto da oxidação anódica o ?-PbO2 que apresentava baixas capacidades de descarga.
Para concentrações das soluções entre 0,5 molL-1 e 5,0 molL-1, o produto da oxidação anódica foi o ?-PbO2 que de forma oposta apresentava altas capacidades de descargas.
Finalmente, para concentrações molares menores que 0,5 molL-1 outra vez o ?-PbO2 foi encontrado. Esses dados podem ser facilmente relacionados com a influência da concentração de íons H+ presentes em diferentes concentrações de ácido, no processo de formação, alertando que para esse processo o controle da concentração do ácido sufúrico é um parâmetro operacional que impacta as características elétricas das placas e portanto da bateria como produto final.
Também nos artigos do Prof.Pavlov encontramos que ele compreende o processo de formação das placas por um mecanismo de reação zonal, começando na interface grade/precursor e sendo capaz de seguir dois caminhos possíveis, buscando sempre as menores concentrações de solução ácida (que dependem das concentrações da solução formadora).
Isso pode ser facilmente compreendido considerando a solução dentro dos poros do material precursor ainda não formado e o fato de que o produto da reação de formação dá como um de seus produtos o ácido sulfúrico.
Como consequência, se a solução formadora for ácida, a reação zonal avançará primeiramente das hastes da grade para dentro da placa e somente depois disso, irá na direção da superfície da placa.
Por outro lado, se a solução de formação for neutra ou alcalina (por exemplo, uma solução de Na2SO4), a reação de zona avançará primeiramente pela superfície da placa e então virá para dentro da placa. Por isso que há patentes registradas onde, na solução de formação, são adicionadas quantidades específicas de solução de Na2SO4 que, em cada caso, diz aumentar a performance da bateria formada de acordo com sua especificação.
Tendo em conta nossa discussão pode-se claramente ver que isso advém do fato que essa ação altera a razão ?/? PbO2 . De acordo com o Prof. D’Alkaine, as estruturas macro e microporosas aparecem no processo de formação, onde a zona de reação parece ser constituída em nível microscópico por uma camada mais fina entre o PbO2 formado e o precursor não formado.
É por isso que a nova morfologia do PbO2 segue a morfologia anterior do precursor. Esta é a razão pela qual o novo material ativo segue quase uma estrutura metassomática do precursor original para a massa ativa positiva que é formada por agregados de partículas interconectadas entre as quais são formados os macroporos.
As partículas dos aglomerados, por sua vez, apresentam em suas superfícies estruturas coralinas que podem ser observadas por microscopia eletrônica de varredura (MEV). Isso confirma a presença de microporos justificada pela origem a uma taxa alta de áreas variáveis que se encontra nos resultados das análises das isotermas de adsorção de gás conhecidas como área B.E.T. Esta alta taxa de áreas variáveis são entendidas como os microporos, fato nunca apontado deste ponto de vista na literatura.
O Prof. D’Alkaine segue sua discussão afirmando que, na verdade, não está claro o que significa no nível microscópico a zona de reação através da qual o precursor se torna PbO2. Em geral, as análises são macroscópicas. No entanto, encontramos alguns artigos que tentam olhar para os fenômenos no nível microscópico, pelo menos no estágio de sulfatação do processo. Como a sulfatação pode preceder a formação (no processo de soaking) ou pode ocorrer em paralelo com o processo de formação, se encontram na literatura trabalhos que, usando micrografias eletrônicas de retroespalhamento, mostram que durante a sulfatação há o desenvolvimento de uma camada de PbSO4 que pode chegar, após 25 h de tempo de imersão, a cerca de 3 ?m de espessura, mas, para tempos menores, pode ser muito menor.
Tudo isso é importante porque é nesse sentido que a sulfatação pode ser vista como um processo de superfície ocorrendo nas superfícies internas dos macroporos dando origem a um filme de PbSO4, como é proposto no presente texto.
PLACAS NEGATIVAS
No caso da massa ativa negativa (NAM), o processo de formação também ocorre em dois estágios e dá origem ao conhecido chumbo esponjoso. A reação que dá origem a este material ainda não foi tão profundamente compreendida. Ela está certamente relacionada com a redução da densidade da passagem do precursor para o chumbo, mas mantendo a macroporosidade do primeiro de uma forma relacionada com a quantidade de fases aquosas retidas no material precursor durante o processo de produção.
Ao mesmo tempo, o processo de sulfatação das paredes internas dos macroporos do precursor, quando transformado em chumbo, parece ser capaz de dar origem a diferentes níveis de rugosidade da superfície interna do macroporo do chumbo esponjoso, permitindo variar a área B.E.T do mesmo jeito encontrado nas placas positivas. Contudo a variação chega a ser muito menor (0,5 a 1,5 m2g-1) para o material NAM do que o que pode ser obtido no caso do material PAM (5,0 a 11,0 m2g-1 de PAM). Acreditamos que a variação da área B.E.T no NAM deve possivelmente corresponder a efeitos de rugosidade e não à microporosidade, como as observações de MEV parecem mostrar.
As Figuras 1 e 2 mostram resumidamente a visão do Prof.Dalkaine dos processos de formação das placas positivas e negativas discutidas acima e a sua visão esquemática dos conceitos de macroporos e microporos (nesse caso, das placas positivas), respectivamente.
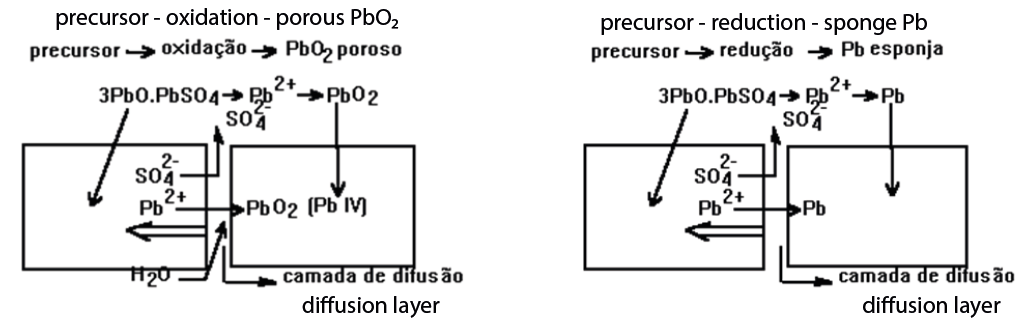
Figura 1: Representação esquemática do mecanismo de formação do (a) material ativo positivo e (b) negativo, a partir do constituinte do material precursor (3BS). O consumo de ácido provoca o movimento dos íons sulfatos que se difundem formando as camadas de sulfato de chumbo. As setas mais largas indicam que a camada de cada material precursor vai diminuindo à medida que aumenta a quantidade de material ativo positivo (PAM) ou negativo (NAM) formado5.
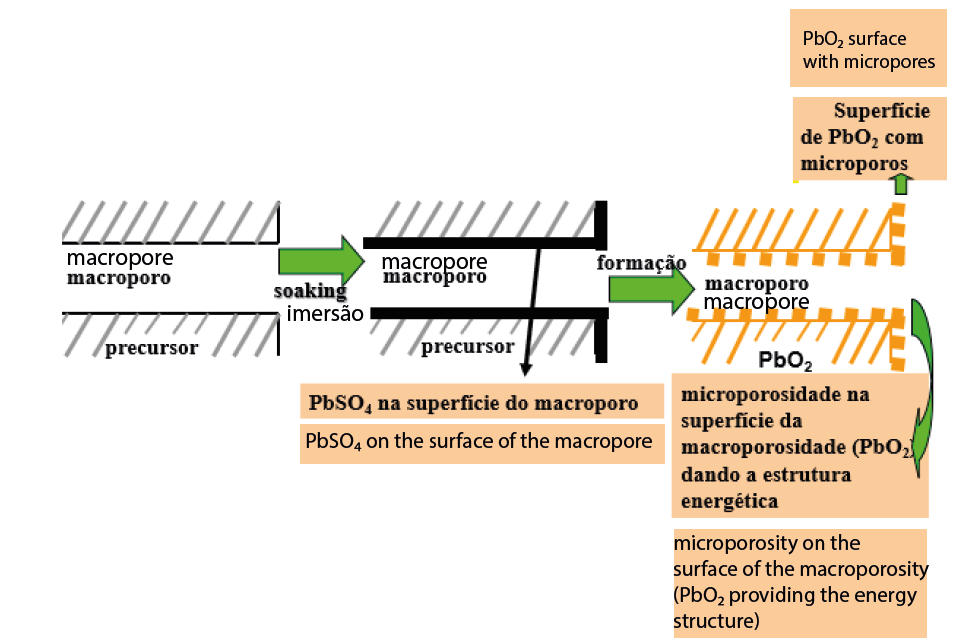
Figura 2 Representação esquemática do mecanismo de formação das placas positivas ressaltando os conceitos de macroporosidade e microporosidade5.
Numa visita aos artigos do Prof.Pavlov6, encontramos também uma esquematização dos dois estágios para caracterizar a formação do NAM, a qual resgatamos agora quase em sua forma original:
• Primeiro estágio. Durante o primeiro estágio, ocorre a redução eletroquímica de PbO e sulfatos básicos de chumbo e o esqueleto de chumbo (rede) é formado. Além desses processos, reações químicas de formação de PbSO 4 também ocorrem. Cristais de PbSO 4 permanecem incorporados no esqueleto de chumbo. Zonas (PbSO 4 + Pb) são formadas em ambas a superfícies da placa e avançam para o interior da placa.
• Segundo estágio. Durante o segundo estágio, ocorre a redução de PbSO4 para Pb e os cristais de chumbo obtidos são depositados na superfície do esqueleto de chumbo em solução
fortemente ácida. O mecanismo das reações químicas e eletroquímicas elementares, bem como suas relações mútuas, foram determinados em alguns trabalhos desse grupo e mostrado que durante a formação, tanto os raios dos poros quanto a porosidade da massa ativa aumentam. Finalizamos esse regaste das visões como ocorre o processo de formação das placas das baterias chumbo-ácido, fazendo um rápido comentário de um trabalho mais recente publicado pelos pesquisadores L. Zerroual e I. Derafa7 (2020) que corroboram com a importância da estrutura do PbO2 para com o desempenho final das placas positivas e, portanto, do desempenho elétrico da bateria chumbo-ácido.
Nesse artigo os autores fazem uma correlação entre a atividade eletroquímica e o tamanho do cristalino de PbO2 obtido quimicamente e eletroquimicamente. As amostras químicas foram obtidas pela dissolução de tetra-acetato de chumbo em água destilada à temperatura ambiente. Enquanto as amostras eletroquímicas foram obtidas diretamente das placas de baterias chumbo-ácido. As descargas das diferentes amostras em soluções de ácido sulfúrico mostraram que a capacidade dos eletrodos formados com PbO2 químico foi independente do tamanho do cristalito. Em contraste, a capacidade do PbO2 eletroquímico diminui com o aumento do tamanho do cristalito.
Referencia:
1D. Pavlov, G. Papazov and V. Iliev, J. Electroch. Soc. 119 (1972) 8-19.
2 D. Pavlov, A. Kirchev, M. Stoycheva and B. Monnahov, J. Power Sources 137 (2004) 288-308.
3 D. Pavlov and E. Bashtavelova. J. Electroch. Soc. 131 (1984) 1468.
4 D. Pavlov and E. Bashtavelova. J. Electroch. Soc. 133 (1984) 241
5 G. A. de O. Brito. XXIV Encontro Nacional de Produtores de Baterias Chumbo-Ácido -ENBAT. Curitiba (2023)
6D. Pavlov. Lead-Acid Batteries: Science and Technology. 1st ed. Elsevier Science; 2011
7L. Zerroual, I. Derafa. Journal: Journal of Inorganic and Organometallic Polymers and Materials, 2020,
n 11, p. 4544-455

Liliane Maria Magalhães de Souza atualmente é professora adjunta do Departamento de Físico-Química do Instituto de Química da Universidade do Estado do Rio de Janeiro (UERJ).
É mestre em Engenharia dos Materiais e Doutora em Físico-química pela Universidade Federal de São Caros, UFSCAR-SP onde iniciou sua formação junto ao Prof. Carlos Ventura D’Alkaine, seu orientador, em 1987, ficando ao seu lado a partir de então e seguindo até sua morte em 2023.
Foram mais de 30 anos de interação e colaboração. Hoje, atua diretamente na área de Engenharia Eletroquímica estudando e desenvolvendo materiais eletródicos com foco nas baterias chumbo-ácido. Contato: liliane_de_souza@yahoo.com










